L'hydrogène en tant que source d'énergie est un élément important pour une économie durable. Non seulement les camions, les trains et les voitures fonctionnent déjà à l'hydrogène grâce aux piles à combustible, mais l'hydrogène est également utilisé dans la production d'acier, l'industrie chimique et le stockage des énergies renouvelables. Il est également utilisé dans la production d'acier, dans l'industrie chimique et comme moyen de stockage des énergies renouvelables.
Toutefois, sa production peut encore être améliorée. Alors que la production à partir du gaz naturel sera probablement exclue à l'avenir, mais qu'elle est actuellement imbattablement bon marché, l'électrolyse nécessite de l'électricité. Et tant que celle-ci n'est pas disponible en abondance à partir de sources renouvelables, la production d'hydrogène est plus inefficace que l'utilisation directe ou, par exemple, l'utilisation de batteries de stockage.
L'approche adoptée par un groupe de recherche de l'université d'État de l'Oregon ( ) n'en est que plus élégante. Une structure faite de métal et d'éléments organiques avec des pores de l'ordre du nanomètre n'a besoin que de la lumière directe du soleil pour extraire de l'hydrogène pur à partir d'eau normale.
Un gain d'efficacité
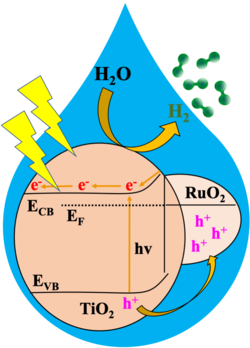
Le principe est appelé photocatalyse. Un processus chimique est déclenché uniquement par l'absorption de photons de la lumière du soleil. La technologie de base est déjà connue. Cependant, les modèles précédents utilisant du zinc, de l'indium ou du titane ne pouvaient utiliser qu'entre 0,3 et 0,7 % de l'énergie solaire incidente pour produire de l'hydrogène.
Grâce à une structure optimisée et à l'utilisation du ruthénium, un métal de transition très rare, l'efficacité pourrait être portée à 10 %, soit 15 à 30 fois plus. Bien que cette valeur soit encore bien inférieure aux taux de conversion d'une cellule solaire commerciale, l'hydrogène est obtenu directement, sans détour et donc sans perte d'énergie supplémentaire.
Les expériences ont permis d'obtenir 10 000 micromoles d'hydrogène par heure et par gramme d'eau. Si les chimistes et les chercheurs en matériaux sont déjà impressionnés, une conversion pourrait aider tout le monde.
Près de 20 % de l'hydrogène contenu dans l'eau peut être dissous en une heure. Cela signifie que 50 litres d'eau suffisent pour obtenir un kilogramme d'hydrogène en une heure. Dans les tests effectués avec de l'eau potable normale, le taux était légèrement inférieur. Environ 60 litres (16 US gal) seraient alors nécessaires.
Une surface d'à peine 100 mètres carrés (1 000 pieds carrés) serait suffisante. Après tout, un kilogramme d'hydrogène suffit pour parcourir près de 100 kilomètres ou chauffer une maison pendant quelques heures.
Top 10
» Le Top 10 des PC portables multimédia
» Le Top 10 des PC portables de jeu
» Le Top 10 des PC portables de jeu légers
» Le Top 10 des ordinateurs portables bureautiques
» Le Top 10 des PC portables bureautiques premium/professionnels
» Le Top 10 des Stations de travail mobiles
» Le Top 10 des Ultraportables
» Le Top 10 des Ultrabooks
» Le Top 10 des Convertibles
» Le Top 10 des Tablettes
» Le Top 10 des Tablettes Windows
» Le Top 10 des Smartphones
» Le Top 10 des PC Portables á moins de 300 euros
» Le Top 10 des PC Portables á moins de 500 euros
» Le Top 25 des meilleurs écrans d'ordinateurs














